蛋白质的性质实验注意事项
来源:网络收集 点击: 时间:2024-07-30其中碳氢被氧化为二氧化碳和水逸出,蛋白质中的氮转化为氨与硫酸结合生成硫酸氯在硫酸中,然后加碱蒸馏,使氨逸出,用硼酸吸收,再以硫酸或盐酸标准溶液滴定。根据酸的消耗量乘以换算系数为蛋白质含量。笔者根据多年来操作经验认为,在检验过程中应注意如下三个环节。一、样品、试剂加入量的控制。
 2/7
2/71.称取试样的多少取决于样品中蛋白质的高低。蛋白质中含氮量较恒定,通常是通过测定食品中氮的含量来确定蛋白质的含量。一般固体样品称取0.2-2.0g,半固体样品称取2—5g,液体样品吸取10-20ml。样品中含氮量低的可增加称样量。
 3/7
3/72.硫酸的加入量,通常加20ml,但试样量如超过5g时,应按每克试样5ml的比例增加硫酸用量。否则试样消化不完全造成结果偏低。3.消泡剂的加入。含脂肪或糖较多的食品在消化时产生大量泡沫,溢出瓶外,造成氮的损失,所以消化前可加入少量消泡齐lj。如:液体石蜡、硅消泡剂等。
 4/7
4/74.催化剂的加入量要适宜硫酸铜是最理想的催化剂,效果好,价格便宜,环境污染小,而且是蒸馏加碱时的指示剂。硫酸钾可加快有机物的分解,使硫酸沸点从34.0℃提高到40.0℃以上,但加入量不能太大,否则温度过高会使铵盐分解而文——胡惠敏造成损失,除硫酸钾外硫酸钠也有同样作用。5.难消化的样品还可适当加入少量过氧化氢,次氯酸钠等氧化剂加速有机物氧化。
 5/7
5/7二、样品消化处理。1.样品一定要移入干燥的凯氏烧瓶中,否则样品易粘在瓶壁上不易消化。加硫酸时应将附在瓶壁上的粉末仔细洗至瓶中,使样品全部消化。还有在消化时注意转动凯氏烧瓶,利用冷凝酸液将附在瓶壁上的碳粒冲下促进完全消化。2.样品与试剂加入摇匀后瓶口应放一小漏斗,将瓶倾斜45。角斜至有小孔的石棉网上,小心加热,避免喷溅。待瓶内试样全部碳化,泡沫完全停止后,再加强火力,并保持瓶内液体微沸,至液体呈澄清透明的蓝绿色后再加热半小时,样品即消化完全。三、蒸馏过程中条件的控制。
 6/7
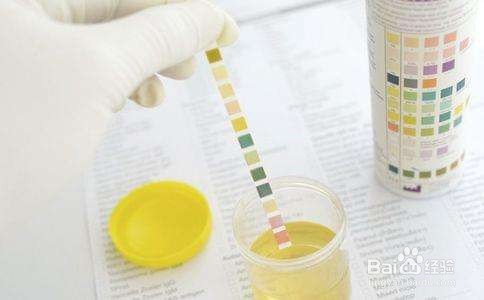
6/71.蒸馏对温度、时间都有要求。热源温度过低直接影响氯的逸出,从而导致结果偏低。蒸馏时间应控制在30分钟左右,时间过少氯放出时间不足,使结果偏低,样品应在温度较高(1000W)的电炉子上蒸馏为宜,达到规定时间后应用PH试纸测出馏出液是否呈中性,若碱性应延长蒸馏时间直至中性。2.氢氧化钠的加入量。在蒸馏过程中,烧瓶内溶液应保持碱性,因此经消化处理样品加氢氧化钠后,瓶内液体在加热沸腾后溶液呈黑色,如果呈兰色,说明氢氧化钠的加入量不足,应补加至分解液呈黑褐色。
 7/7
7/73.硼酸作为吸收液。由于硼酸是极弱的酸,只起吸收氯的作用,不影响碱滴定,但要注意硼酸吸收液温度不应超过40℃,否则氯吸收减弱,造成损失。4.蒸馏装置不能漏气。蒸馏过程中不能停火断气避免发生倒吸,蒸馏完毕先将蒸馏出1:3离开液面,继续蒸馏1分钟,将附着在尖端的吸收液完全洗入吸收瓶内,否则吸收液体将发生倒吸造成意外。5.在滴定过程中一定要将滴管中的气泡赶出,使之在0刻度线时开始滴定,滴定时不要过快,以免达到终点时不好控制。总之,在检验过程中注意以上几点,才能减少误差,确保俭测结果与真实值一致
 注意事项
注意事项注意实验的安全
蛋白质实验版权声明:
1、本文系转载,版权归原作者所有,旨在传递信息,不代表看本站的观点和立场。
2、本站仅提供信息发布平台,不承担相关法律责任。
3、若侵犯您的版权或隐私,请联系本站管理员删除。
4、文章链接:http://www.1haoku.cn/art_1035522.html
 订阅
订阅